El principal propósito de un laboratorio clínico es proporcionar información relevante para la prevención, diagnóstico y pronóstico de enfermedades; y es a partir de los resultados emitidos por el Laboratorio Clínico que se toman más del 70% de las decisiones médicas. La calidad en la atención médica, se encuentra precisamente en el Laboratorio Clínico donde es clara la necesidad de contar con sistemas de gestión de calidad y de competencia técnica, que incluyan el diseño e implementación de un plan estratégico que incorpore la selección de metas analíticas, medibles, alcanzables y retadoras que contribuyan a al cumplimiento de los requisitos normativos y de los objetivos definidos por la institución, enfatizando la relevancia médica, la revisión de la trazabilidad metrológica de los métodos analíticos, la evaluación de indicadores de competencia y la toma de acciones que contribuyan a la disminución de los riesgos y errores asociados a la liberación de resultados clínicos.
Todos los resultados generados en un laboratorio pueden impactados principalmente por dos factores: la variabilidad biológica (VB) del analito en estudio y la variabilidad analítica (VA) del método.
Para que un resultado de laboratorio cumpla con las metas analíticas establecidas, es necesario que la variabilidad analítica del método sea inferior a la variabilidad biológica del analito y para que este criterio se cumpla es necesario que se efectúen las estrategias necesarias y adecuadas para disminuir la variación analítica al máximo, mediante programas de control de calidad que favorezcan el control adecuado control de los errores sistemáticos y errores aleatorios.
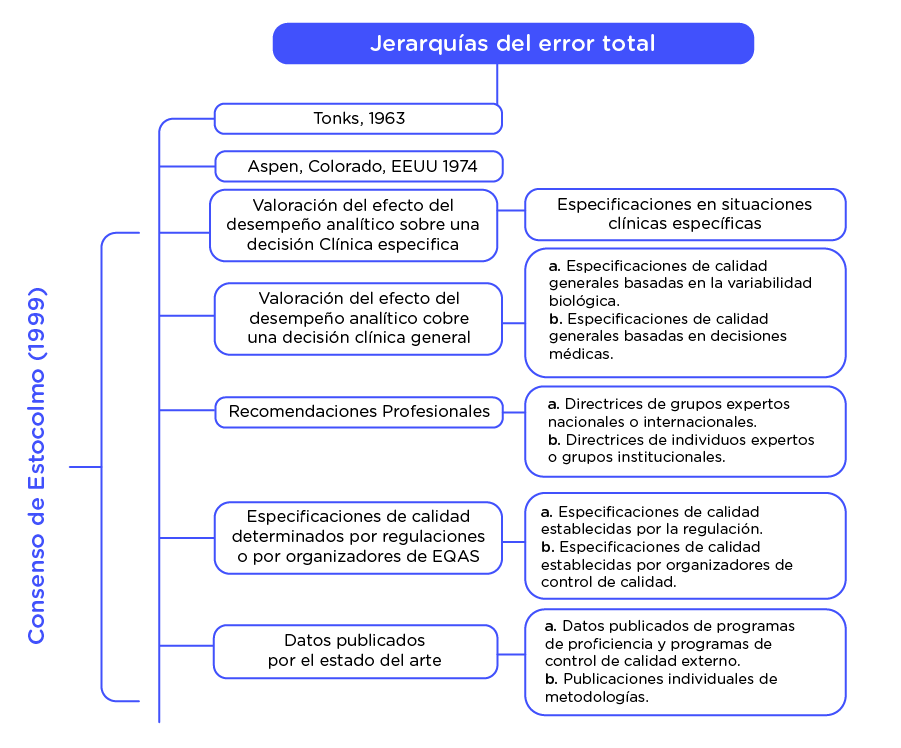
A lo largo de la historia, se han formulado diferentes modelos y estudios a partir de los cuales se establecen las metas de calidad, iniciando por los criterios definidos en el año 1963 por David Tonks quien sugirió que los errores permitidos deben ser relacionados con el ancho del intervalo de referencia y definió que el error no debe ser mayor a un cuarto del rango normal, años más adelante se presentaron otras fuentes como por ejemplo:
Barnet (1968): Recomendaciones de desempeño analítico basadas en opiniones de expertos y laboratoristas.
Fraser (1981-1983): Desempeño basado en estado del arte.
CAP 80`s: Uso de variabilidad biológica para definir desempeño y metas para precisión para técnicas de screening.
Fraser/ Ricos (1997): Metas basadas en variabilidad biológica Mínimas, Deseables y Óptimas.
CLIA `88: Publicación final en 1992 y actualizado el 2003. Regulatorio en EEUU, Criterios de desempeño para Proficiency Testing, basado en estado del arte en 1988.
CLSI 2002: Medición del error total (EP21-A) y hacia el 2006: Control estadístico de técnicas cuantitativas (diseño de reglas de QC según error total) (C24-A3).
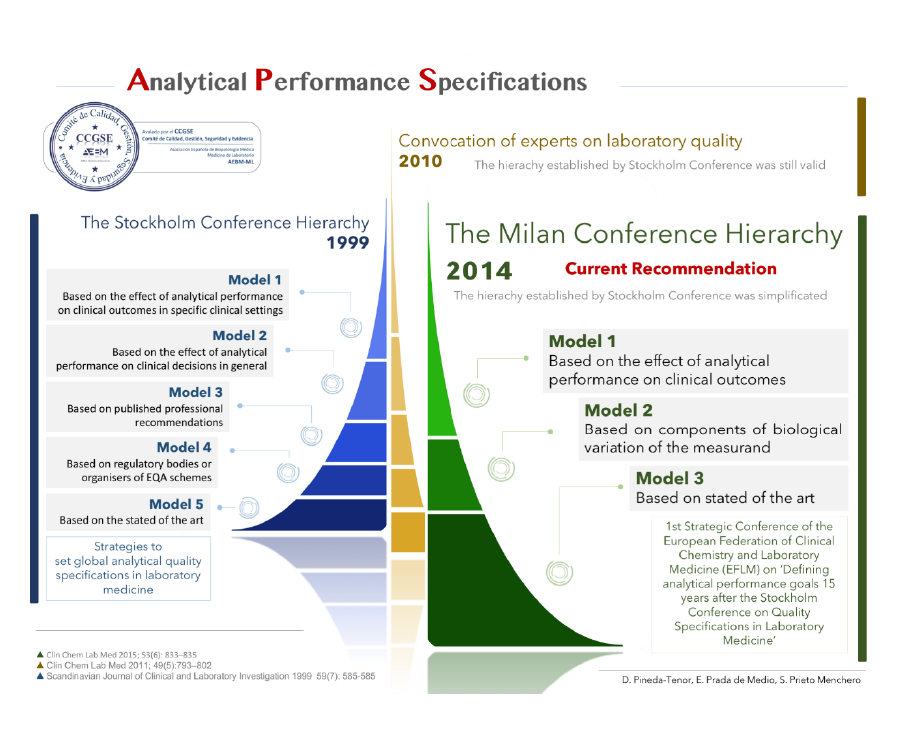
En noviembre de 2014, se celebró en Milán la primera Conferencia Estratégica de la European Federation of Clinical Chemistry and Laboratory Medicine (EFLM) sobre “Definición de Objetivos de Rendimiento Analítico”, quince años después de la Conferencia de Estocolmo sobre Especificaciones de Calidad en el Laboratorio Clínico.
Una revisión de la jerarquía original de 1999 fue llevada a cabo por 215 participantes procedentes de 41 países. En este nuevo consenso, la jerarquía se presenta simplificada, presentando 3 modelos diferentes para definir las especificaciones de calidad.
Pese a que la jerarquía propuesta originariamente en Estocolmo en 1999 continúa siendo de utilidad, el más reciente consenso de Milán de 2014 simplifica el concepto, priorizando la definición de especificaciones analíticas basadas en el efecto del rendimiento sobre las situaciones clínicas concretas (Modelo 1) o la variabilidad biológica del mensurando (Modelo 2) y las especificaciones obtenidas basadas en el estado del arte (Modelo 3).
En el año (2019-2022), los Centros de servicios Medicaid y Medicare emitieron los cambios propuestos las regulaciones de CLIA y fueron publicadas en el Registro Federal de EU para expandir la lista de analitos regulados (de 67 a 101) y definir nuevos criterios de rendimiento aceptables para las pruebas de aptitud (PT), aumentando el número de analitos incluidos.
En el año 2024 se realiza nueva actualización de las regulaciones en la cual se prevé implementar nuevos objetivos (23 cambios con respecto a 2019) para analitos como ALT, AST, Bilirrubina Total, CK-MB, Glucosa, HbA1c, C3, IgA, CEA entre otros.
La existencia de metas analíticas es amplio y variado. Los laboratorios cuentan con diversas fuentes para definir sus objetivos analíticos contra las cuales comparan sus resultados del desempeño en términos de precisión (CV%), veracidad (%Sesgo) y Error Toral. Dentro de estas metas, las más utilizadas son las definidas en el nivel jerárquico más bajo, establecidas por organizaciones como, por ejemplo:
- Clinical Laboratory Improvement Amendments (CLIA)
- Rilibak
- Sociedad Española de Química Clínica (SEQC),
- Variabilidad Biológica de las concentraciones de los analitos en un mismo individuo alrededor de su punto homeostático in vivo y a la variación de las concentraciones entre individuos de condiciones similares (variación intra e interindividual).
Adicional, los laboratorios clínicos a nivel mundial han incorporado como parte de sus metas analíticas de calidad el modelo Seis Sigma que tiene como fundamento la cuantificación de los errores o defectos, lo que en calidad analítica cuando se supera una meta analítica que ha seleccionado el laboratorio, se considera un defecto. La calidad de un proceso se mide en la escala σ, con un criterio de 3 σ como el nivel mínimo.
Para finalizar es importante recordar que la calidad en el laboratorio clínico no es un proceso estático y que debe ser sujeto a la implementación de estrategias de mejora permanentemente. La mejora continua de la calidad basada en Six Sigma y la definición de metas analíticas, proporciona la metodología adecuada para solucionar los errores y disminuir los riesgos, lo que implica el compromiso de las instituciones desde la planeación estratégica con la gestión de la calidad.
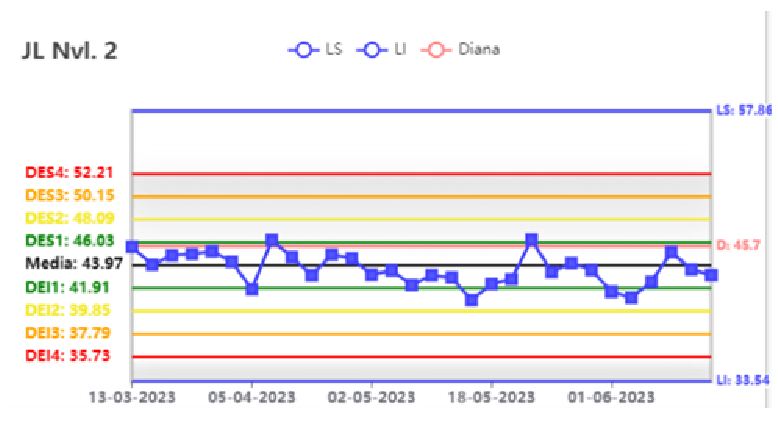
El objetivo de todo programa de control de calidad es asegurar por parte del laboratorio la generación de resultados clínicamente útiles y confiables, por lo cual cobra importancia contar con herramientas que mejoren los procesos de control de la fase analítica y que impacten positivamente en la toma de decisiones hacia la mejora continua.
¿Quieres saber más sobre control de calidad en el laboratorio? Pregunta a tu ejecutivo de cuenta o escríbenos a serviciocliente@annardx.com
Bibliografía
1.C. Ricos, C. Perich, J. Minchinela, V. Alvarez, M. Simón, C. Biosca. Application of biological variation: A review. Biochem Med., 19 (2009), pp. 250-259
2.J.G. Milan. The new hierarchy: Update from the EFLM strategic conference on defining analytical performance goals Quality specifications for QC and QAP. Pathology., 48 (2014), pp. S16
3.J. Westgard. Six Sigma basics. En: Sig Sigma quality design and control. WesTgard QC, (2006)