La espectrometría de masa da origen en 1987 mediante el descubrimiento del electrón, por el físico británico Joseph John Thomson, quien bajo este hallazgo sentó las bases para la separación de partículas cargadas en función de su masa y carga. En 1912 bajo estas bases J.J. Thomson diseña el primer espectrómetro de masas, en el cual permitió la separación de los isótopos de neón en función de su relación masa/carga (m/z).

Por otro lado, la cromatografía de ultra alta eficiencia (UHPLC) es la evolución de la cromatografía líquida de alta eficiencia (HPLC), la cual dio origen en 1901 por el botánico ruso Mikhail Tsvet, quien desarrolló la primera columna de cromatografía, la cual separaba los pigmentos en bandas de colores, lo que básicamente sentó las bases de la cromatografía, posteriormente en el año de 1960 se diseñó la cromatografía líquida de alta eficiencia (HPLC) y en el 2004 se elabora un equipo capaz de soportar presiones altas, mejorando la eficiencia y rapidez en la separación de compuestos, este nuevo diseño fue nombrado como UHPLC.
En la actualidad la cromatografía es una técnica fundamental en el análisis fisicoquímico, permitiendo la separación, identificación y cuantificación de compuestos en una muestra. Entre las metodologías más avanzadas se encuentran la cromatografía líquida acoplada a espectrometría de masas (LC-MS) y la cromatografía líquida de ultra alta eficiencia (UHPLC), las cuales han revolucionado diversas disciplinas científicas y tecnológicas como:
- Análisis de fármacos y metabolitos.
- Detección de sustancias en toxicología y dopaje.
- Estudios y análisis medioambientales.
- Ciencias biológicas.
La cromatografía líquida acoplada a espectrometría de masas (LC-MS) combina dos técnicas analíticas: la cromatografía líquida (LC), que permite la separación de los compuestos, y la espectrometría de masas (MS), que facilita su identificación y cuantificación con alta precisión. Esta técnica ha cobrado gran importancia en campos como la farmacología, la biotecnología y la toxicología; el principio de la LC-MS radica en la inyección de una muestra líquida en una fase móvil, que se transporta a través de una columna cromatográfica donde los compuestos se separan en función de su afinidad con la fase estacionaria.
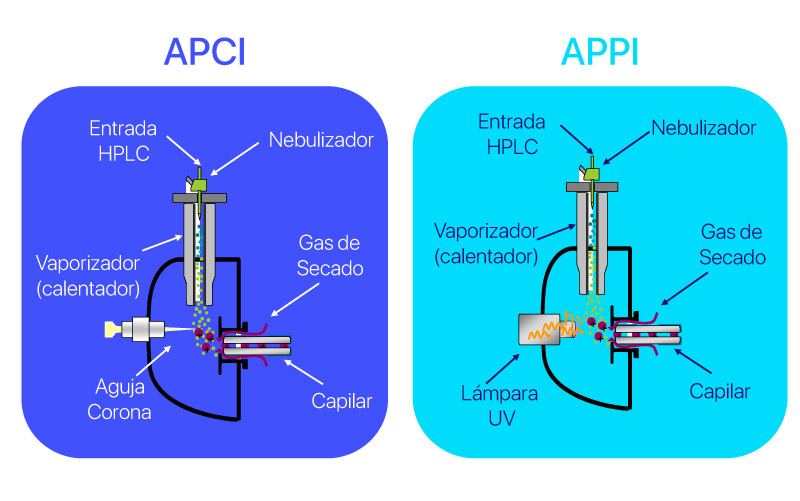
Posteriormente, las moléculas son ionizadas mediante diversas técnicas, como la ionización por electropulverización (ESI) o la ionización química a presión atmosférica (APCI), y luego se analizan en el espectrómetro de masas, proporcionando información sobre su estructura molecular.
La eficiencia de un equipo o instrumento LC-MS o un UHPLC-MS se ve incrementada con el uso de disolventes más limpios. En este contexto, un disolvente grado HPLC no es la opción más conveniente para su uso en LC-MS/UHPLC-MS, ya que algunas impurezas no detectadas por espectroscopia UV pueden interferir en la espectrometría de masas. Por el contrario, el uso de disolventes limpios y aptos para equipos de LC-MS o UHPLC-MS evita obstrucciones en los equipos y reduce los mantenimientos.

Las impurezas metálicas a nivel de ppm que no afectan a la cuantificación de un HPLC convencional pueden afectar o distorsionar su espectro de masas, modificando la abundancia de los iones moleculares de interés generando complicación en la interpretación de un analista. A continuación, veremos dos espectros de masas de un mismo analito, donde se observa claramente las diferencias al usar acetonitrilo y agua de calidad HPLC y LC-MS. Cabe aclarar que el analito analizado es el péptido gastrina humana y el ion molecular (M+2H)2+, deben aparecer a 1050 m/z.
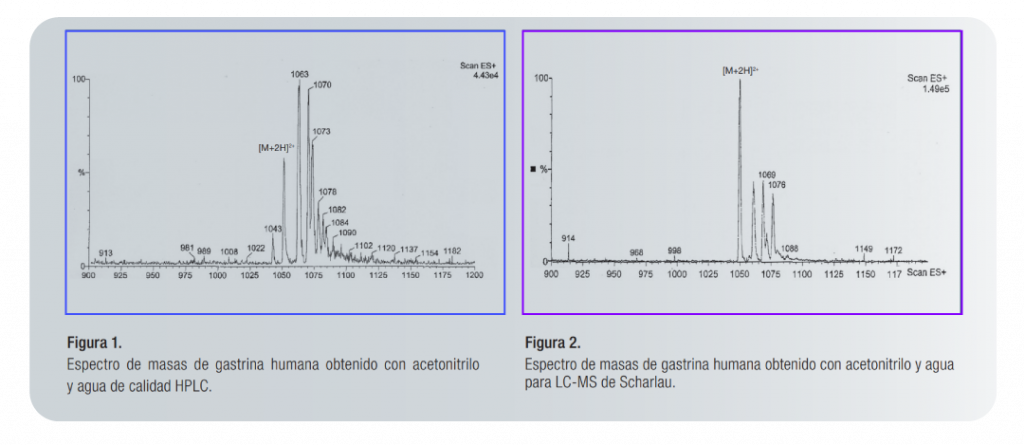
En la figura 1, el pico deseado está enmascarado por otros picos correspondientes a aductos del péptido con otros metales alcalinos ([M+Na+H]2+, m/z es 1063 o [M+K+H]2+, m/z es 1070), debido al empleo de disolventes de calidad HPLC. A diferencia de la figura 2, la cual, muestra un espectro claro y limpio, correspondiente al ión deseado [M+2H]2+, gracias al uso de acetonitrilo y agua para LC-MS, estos reactivos usados fueron de la marca Scharlau, los cuales ofrecen beneficios como:
- Espectros más simples y limpios.
- Evita la formación de aductos no deseados de impurezas metálicas.
- Alargar la vida útil de las columnas cromatográficas.
- Evita obstrucciones del equipo.
- Ahorrar en el mantenimiento de sus equipos.
Por tal razón ANNAR Health Technologies cuenta en su portafolio con solventes marca SCHARLAU, desarrollados para reducir la cantidad de impurezas no deseadas, todas las botellas de solventes LC-MS y UHPLC-MS han sido sometidas a un tratamiento especial de pasivado que impide la migración de trazas metálicas del vidrio al disolvente. Además, los solventes y mezclas para LC-MS/UHPLC-MS cumplen con todos los requisitos para la obtención de resultados y análisis, precisos y confiables, lo que asegura:
- Bajo contenido de impurezas Metálicas.
- Microfiltrado a 0,1 µm.
- Mínimo nivel de acidez y alcalinidad.
- Bajo contenido agua.
- Bajo nivel de impurezas no volátiles.
- Impurezas controladas por LC-MS o UHPLC-MS.
- Certificado de análisis por cada lote.
En resumen, la cromatografía LC-MS y UHPLC-MS han revolucionado el campo del análisis químico, ofreciendo técnicas de separación y detección de alta precisión y rapidez, la eficiencia de estas técnicas depende en gran parte de la calidad y pureza de los solventes químicos. Su impacto en múltiples campos científicos e industriales demuestran su relevancia y a medida que estas tecnologías sigan evolucionando, su integración con nuevas herramientas digitales y automatización continuará mejorando la eficiencia y accesibilidad del análisis químico; ANNAR seguirá a la vanguardia ofreciendo los reactivos químicos óptimos y eficientes de Scharlau, buscando consolidarse como pilar fundamental en la ciencia analítica moderna.
¿Quieres saber más sobre solventes químicos para cromatografía?
Consulta con tu ejecutivo de venta o escríbenos a serviciocliente@annardx.com
Bibliografía









