¿Sabías qué?
Desde que se sancionó la ley 1980 en Julio del 2019, se empezó a instaurar el programa de Tamizaje Neonatal Básico en Colombia, en donde uno de los cambios más significativos es el cambio de la muestra de sangre de Cordón a Sangre de Talón.
Te contamos sobre los aspectos más importantes que debemos tener en cuenta en la fase preanalítica:
Papel de filtro:
De acuerdo con la guía internacional CLSI NBS-01-A6-2013, el consenso de APHL y la norma ASTM (16) el papel de filtro adecuado para realizar las pruebas de tamizaje neonatal es el Whatman 903 y el Ahlstrom 226 ya que debe cumplir con los requerimientos de material, densidad, peso, pH, cenizas, resistencia y absorbancia, que garanticen la capacidad de absorción, la homogeneidad y el volumen de retención de la muestra.

Tarjeta de Tamizaje Neonatal:
El modelo proporcionado por el INS en la actualización técnica operativa para laboratorios de tamizaje neonatal, contiene información de la madre y sus antecedentes médicos, información del recién nacido, condiciones del nacimiento, hora de toma de muestra, hora de nacimiento y pruebas solicitadas dentro de otros.

Muestra:
Sangre de talón en papel de filtro de acuerdo con la Guía de práctica Clínica para la Detección de anomalías congénitas en el recién nacido – Sistema General de Seguridad Social en Salud – Colombia-Guía 03- (2013) se debe recolectar la muestra entre 24 y 72 horas una vez el neonato haya recibido alimentación.

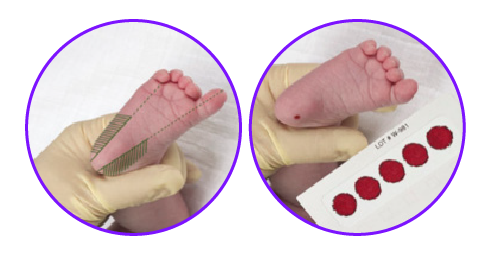
Toma de muestra:
Debe ser por parte personal entrenado, Se realiza en la zona externa del talón del recién nacido, se utiliza una lanceta automática que realiza una punción no mayor de 2mm de profundidad para RN >2500gr de peso y para prematuros o RN <2500gr de peso se emplea una lanceta con un corte de 0,85mm. Según la guía CLSI H04-A6-2008. El goteo debe ser libre y se deben tomar 5 o 6 gotas de muestra. Se debe dejar secando la muestra de 3 a 4 horas.
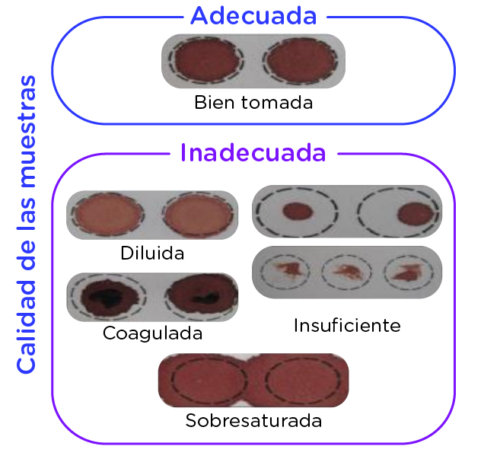
Calidad de la muestra:
Es fundamental que las muestras no estén sobresaturadas, diluidas, coaguladas o insuficientes porque estos son factores que afectan los resultados, ya sea incrementando los valores de la concentración de los analitos e induciendo a falsos positivos o por dilución se pueden obtener resultados Falsos negativos.
Almacenamiento de las muestras:
De acuerdo con la guía internacional CLSI NBS-01-A6-2013 las muestras se deben conservar en bolsas metalizadas con cierre hermético y con perlas de control de humedad para garantizar la estabilidad de los analitos. Según el CDC las muestras pueden ser estables hasta por 2 años si se almacenan a temperaturas entre 4°C – 8°C y por más de dos años si se congelan entre -20°C y -70°C.

Transporte:
Según la Guía sobre la reglamentación relativa al transporte de sustancias infecciosas 2019-2020, publicado por la OMS, se tiene en cuenta el numeral 4.6 EXENCIONES para sangre seca en papel de filtro, pueden ser enviadas o transportadas por correo, sin expectativas de exposición ocupacional a sangre u otro material infeccioso. Deben seguirse las precauciones universales para el procedimiento de embalaje.
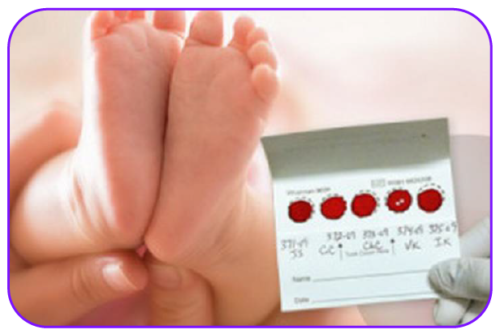
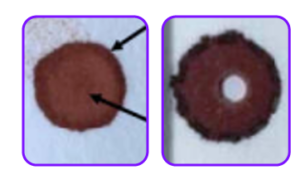
Lugar del ponchado de la muestra:
Es fundamentar elegir el sitio donde la muestra tiene una distribución homogénea de los hematíes en el centro de la mancha, hay que evitar obtener spots de la periferia de la mancha de sangre ya que allí hay una mayor concentración de hematíes y se pueden obtener falsos positivos o resultados no reproducibles.
Importante
- Estos biomarcadores son susceptibles a condiciones ambientales – variaciones de temperatura y humedad.
- En lugares cálidos o con temperaturas elevadas se sugiere el envío de las muestras refrigeradas para evitar Falsos Negativos.
- La calidad de las muestras tiene un papel fundamental en la veracidad de los resultados obtenidos en los programas de tamizaje neonatal.
- La mala calidad de las muestras genera re llamados y demora en los resultados lo que puede ser determinante en la calidad de vida del recién nacido.
- Fallas en la toma de muestra o muestras deficientes generan reprocesos en el laboratorio y sobrecostos.

Referencias
https://www.ins.gov.co/TyS/programas-de-calidad/Documentos%20del%20Programa%20TSH%20Neonatal/6%20Cuidados%20con%20las%20DBS%20Dra.%20Dora%20Robayo.pdf
Ley 1980 de 2019. Por medio de la cual se crea el programa de tamizaje neonatal en Colombia. 26 de julio de 2019. D.O. No. 51026.
Use of Dried Blood Spot Specimens to Monitor Patients with Inherited Metabolic Disorders Stuart J. Moat 1,2, *, Roanna S. George 3 and Rachel S. Carling. 2020
ins.gov.co/BibliotecaDigital/Actualizacion-tecnica-operativa-tamizaje-neonatal.pdf
Lineamiento nacional para la coordinación e implementación del tamizaje neonatal por laboratorio en Colombia. En cumplimiento de la Ley 1980 de 2019. [Instituto Nacional de Salud]. Mayo del 2022. 21.
Clinical and Laboratory Standard Institute. 2013. CLSI. Blood collection on filter paper for newborn screening programs; Approved standard – sixth edition. CLSI document NBS01-A6. Wayne, PA.
Standard specification for laboratory filter papers. American Society for Testing and Materials (ASTM). E832-81(2019). DOI:10.1520/E0832-81R19.
Ministerio de Salud y Protección Social – Colciencias Guía de práctica clínica. Detección de anomalías congénitas en el recién nacido. 2013 – Guía No.03. [ En línea] [Consulta: 2022-06-04] Recuperado de: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/INEC/IETS/GPC _Completa_Anom_Conge.pdf