PD-L1 IHC 22C3 PharmDx es el único diagnóstico complementario probado en ensayos clínicos indicado como ayuda para identificar pacientes con cáncer de pulmón de células no pequeñas (CPNM) para el tratamiento con KEYTRUDA (pembrolizumab). Esta guía de interpretación se proporciona como una herramienta para ayudar a guiar a los patólogos y al personal de laboratorio a lograr resultados correctos y reproducibles en la evaluación de la expresión de PD – L1 en muestras de pacientes diagnosticados con CPNM, fijadas con formalina e incluidas en parafina y escaneadas mediante un Sistema de Inteligencia Artificial ASI. La expresión de PD – L1 puede ayudar a identificar pacientes para inmunoterapia anti – PD-1.

La expresión de la proteína PD – L1. Se determina mediante el uso del puntaje de proporción tumoral (TPS), que es el porcentaje de células tumorales viables que muestran tinción de membrana parcial o completa a cualquier intensidad. Se debe considerar que la muestra tiene expresión de PD – L1 si el TPS es ≥ 1 % y alta expresión de PD – L1 si el TPS es ≥ 50 %.
PD – L1 IHC 22C3 PharmDx. Se considera un ensayo cualitativo; por lo tanto, el resultado puede diferir de un médico patólogo a otro, sin embargo, el estado de diagnóstico mediante la expresión de PD – L1 requiere la determinación del porcentaje de células tumorales teñidas. Siendo muy acertado el Sistema de Inteligencia Artificial (ASI) que es una herramienta digital creada para disminuir estos errores. Las muestras de tejido de cáncer de pulmón de células no pequeñas que se analizan para detectar la expresión de PD – L1 se califican y se dividen en tres niveles según una puntuación de proporción de tumor (TPS):
- TPS < 1%: No hay expresión de PD – L1.
- TPS 1 – 49%: expresión de PD – L1.
- TPS ≥ 50%: Alta expresión de PD – L1.
Los niveles de expresión de PD – L1 se utilizan para informar la elegibilidad del paciente para el tratamiento con KEYTRUDA.
La vía PD – 1 / PD – L1. Controla el sistema inmunológico respuesta en el tejido normal:
El ligando de muerte programada 1 (PD – L1) es una proteína transmembrana que se une al receptor de muerte programada 1 (PD – 1) durante la modulación del sistema inmunitario. El receptor PD-1 se expresa normalmente en las células T citotóxicas y otras células inmunitarias, mientras que el ligando PD – L1 se expresa normalmente en las células normales. Las células normales utilizan la interacción PD – 1 / PD – L1 como mecanismo de protección contra el reconocimiento inmunitario inhibiendo la acción de las células T (Figura 1). La inactivación de las células T citotóxicas regula a la baja la respuesta inmunitaria, de modo que la célula T inactiva se agota, deja de dividirse y puede acabar muriendo por muerte celular programada o apoptosis.
El tumor se escapa. Detección mediante la vía PD – 1 / PD – L1:
Muchas células tumorales son capaces de aumentar la expresión de PD – L1 como mecanismo para evadir la respuesta inmunitaria natural del organismo. Las células T activadas reconocen el marcador PD – L1 en la célula tumoral, de forma similar a la de una célula normal, y la señalización de PD – L1 hace que la célula T quede inactiva (Figura 2). La célula tumoral escapa al ciclo inmunitario, continúa evitando la detección para su eliminación y es capaz de proliferar.
La terapia anti – PD – 1 posibilita la respuesta inmunitaria contra los tumores:
LLAVETRUDA® (pembrolizumab) es un inmunoterapéutico contra el cáncer anti – PD – 1 que bloquea la interacción PD – 1/ PD – L1 entre las células tumorales y las células T activadas (Figura 3). Cuando la célula tumoral no puede interactuar con la célula T activada, el sistema inmunitario permanece activo, lo que ayuda a prevenir la inmunosupresión.
PD-L1 IHC 22C3 pharmDx detecta PD – L1 en muestras de CPCNP:
La regulación positiva y la detección de PD-L1 en las células tumorales es un biomarcador de la respuesta a la terapia anti-PD-1. PD – L1 IHC 22C3 pharmDx fue el único diagnóstico complementario utilizado en los ensayos clínicos KEYTRUDA (KEYNOTE-010 y KEYNOTE-024), que investigaron la eficacia clínica de KEYTRUDA en pacientes con CPNM. KEYTRUDA es un anticuerpo monoclonal humanizado bloqueador de PD-1.
Evaluar la tinción y determinar la puntuación de la proporción del tumor
Definición de tumor Puntuación proporcional (TPS):
La puntuación de proporción tumoral es el porcentaje de células tumorales viables que muestran tinción de membrana parcial o completa (≥ 1+) en relación con todas las células tumorales viables presentes en la muestra (positivas y negativas).
TPS = # Células tumorales positivas para PD – L1 / (Número total de células tumorales PD-L1 positivas + PD – L1 negativas).
Evaluación de la tinción de PD – L1
Califique la tinción parcial o completa de la membrana celular (≥ 1+) que se percibe como distinta a la tinción citoplasmática. Excluya la tinción citoplasmática de la puntuación.
Califique únicamente las células tumorales viables. Excluya todas las demás células de la calificación: células inmunes infiltradas, células normales, células necróticas y restos.
Directrices y métodos Para determinar el tumor Puntuación proporcional:
- Con un aumento bajo, examine todas las áreas tumorales bien conservadas. Evalúe las áreas generales de células tumorales positivas y negativas, teniendo en cuenta que la tinción parcial de la membrana o la tinción de membrana 1+ pueden ser difíciles de ver con un aumento bajo. Asegúrese de que haya al menos 100 células tumorales viables en la muestra.
- Con aumentos mayores, incluidos 10x, 20x y 40x, observe todas las áreas del tumor con y sin tinción de la membrana celular.
- En esta etapa de trabajo con múltiples aumentos, el análisis primario implica:
- Distinguir las células tumorales de las células inmunes asociadas al tumor.
- Determinación de áreas tumorales positivas y áreas tumorales negativas.
- Determinación de tinción parcial y completa de membrana ≥ 1+.
- Calcule la puntuación de proporción de tumor evaluando el porcentaje de células tumorales positivas para PD – L1 en relación con todas las células tumorales viables presentes en la muestra.
Nota: Considere cuidadosamente el área total del tumor sin ninguna tinción perceptible y convincente de la membrana celular.
Asegúrese de excluir las células inmunes y el tejido necrótico se puntúan Las siguientes consideraciones pueden ayudar a distinguir las células tumorales de las células inmunes:
- Las células inmunes pueden tener núcleos más pequeños que las células tumorales.
- Los macrófagos pueden contener partículas pigmentadas en su citoplasma.
- Los macrófagos pueden tener una distribución dispersa.
- Los macrófagos pulmonares están presentes en el espacio alveolar.
Pautas de puntuación:
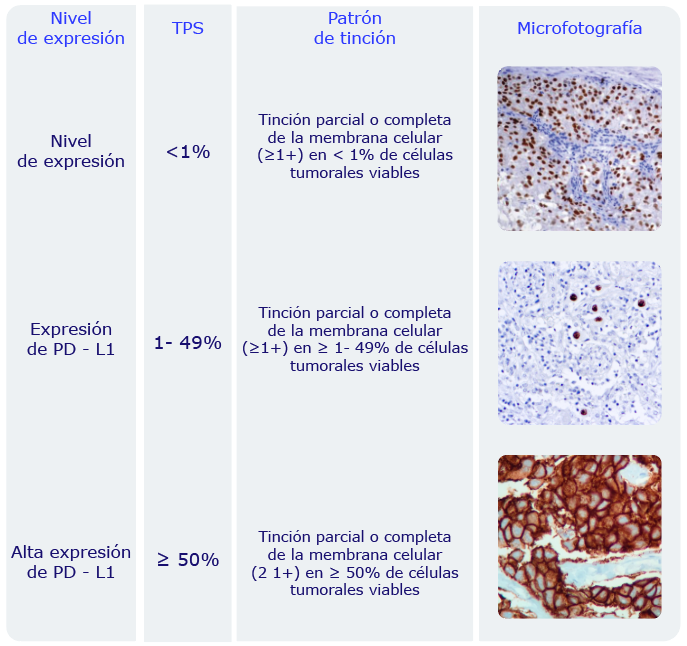
Métodos sugeridos para determinar el TPS:
Agilent recomienda que la puntuación se realice en el contexto de la experiencia previa del patólogo y su mejor criterio a la hora de interpretar las tinciones de inmunohistoquímica. Ofrecemos dos ejemplos diferentes de técnicas que se pueden utilizar al considerar varios patrones de tinción para determinar las respectivas puntuaciones de proporción tumoral.
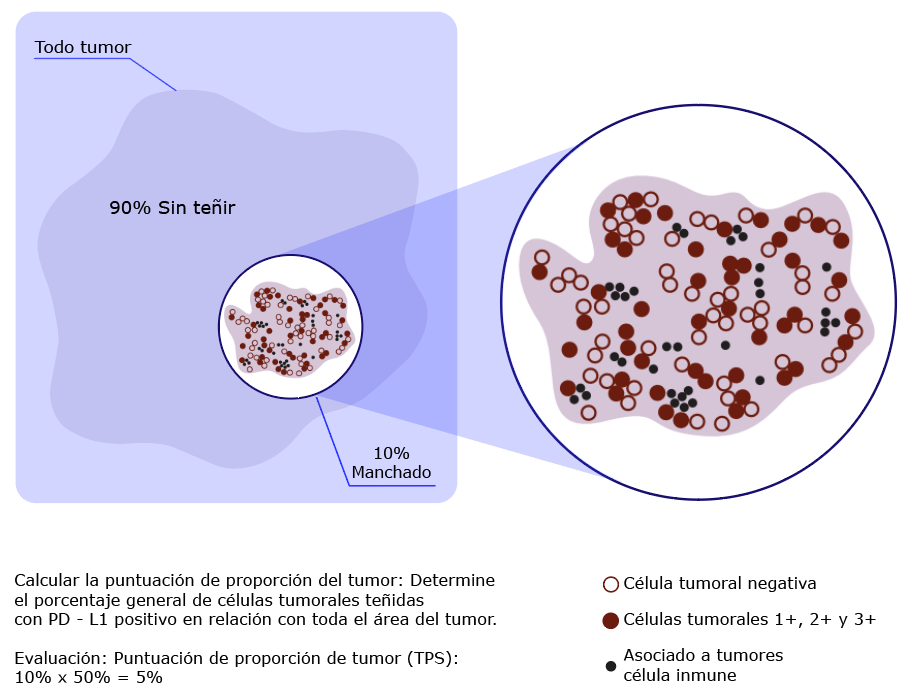
Ejemplo 1: Cálculo de la puntuación positiva combinada en un área tumoral pequeña con tinción.
Con un aumento menor: evalúe el área del tumor para detectar cualquier tinción perceptible y convincente de la membrana celular ≥ 1+.
Evaluación: 10% del área con tinción, 90% del área sin tinción.
Con mayor aumento: evalúe el área de tinción para estimar el porcentaje de células tumorales que son PD-L1 positivas y PD-L1 negativas.
Evaluación: El 50% de estas células son PD-L1 positivas.
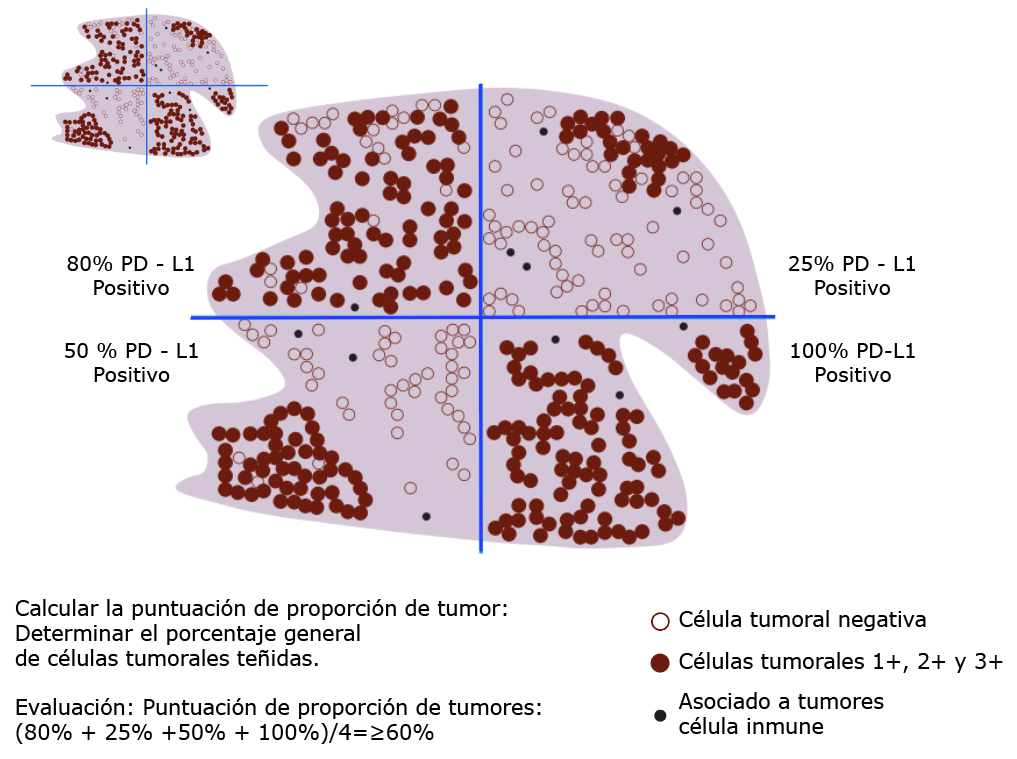
Ejemplo 2: Cálculo de la puntuación de proporción tumoral en un área tumoral heterogénea.
Con menor aumento: divida visualmente el área del tumor en secciones.
Con mayor aumento: observe las áreas tumorales con tinción de la membrana celular para ver el porcentaje de células teñidas en cada sección.
Evaluación: Tinción de células tumorales en cada una de las cuatro secciones respectivas: 80%, 25%, 50%.
Sistema de Inteligencia Artificial (ASI) applied spectral imaging
Actualmente, la inteligencia artificial está transformando la manera en que se abordan nuevos desafíos, y es que, el estudio y desarrollo de este campo, pone en evidencia las ventajas que trae consigo. Hace tiempo que se utilizan técnicas basadas en inteligencia artificial para realizar ciertas tareas, sin embargo, ha sido recientemente con el desarrollo de inteligencias artificiales generativas, cuando se comienza a entender el potencial presente en este campo aún en desarrollo. Además, entre sus principales técnicas, existe una de utilidad especial conocida como visión artificial, que consiste en darle a un ordenador la capacidad de analizar imágenes y mostrar lo que ocurre en ellas. Esto resulta de interés, ya que hay imágenes que presentan características imperceptibles al ojo humano, pero que una máquina puede procesar. En este caso se tiene como ejemplo las imágenes médicas, que en muchos casos presentan patrones que, al ser identificados, pueden servir para conocer en mejor profundidad qué le ocurre al paciente. Esta habilidad de analizar imágenes, junto con la ventaja de tratarse de una máquina, hacen de la inteligencia artificial una solución eficiente para muchos problemas, eliminando el error derivado del factor humano. Por otro lado, aporta a la comunidad científica otro punto de vista cuando se trata de nuevos retos e investigaciones. Por tanto, el principal objetivo de la presente guía es el desarrollo y evaluación mediante algoritmos que sean capaces de reconocer y diferenciar tanto las células tumorales como las no tumorales, además que el sistema sea capaz de diferenciar la no marcación, la marcación débil y la marcación fuerte que puedan interpretarse mediante mapas de calor emitiendo resultados cada vez más precisos mediante el sistema APPLIED SPECTRAL IMAGING (ASI) especializado en el análisis de imágenes médicas para determinar el estado de una proteína específica, el PD- L1.
El Sistema ASI. Mejora las capacidades de gestión de imágenes del laboratorio de patología con la plataforma de patología digital independiente del escáner de ASI y beneficia la visualización, la comparación de tejidos y el análisis de imágenes adquiridas en escáneres de terceros.
El sistema toma una serie de fotografías en diferentes objetivos (acercamientos) y luego las recopila como si se tratará de un Google Maps. El sistema reconstruye las imágenes y le permite al usuario navegar por cualquier parte del tejido, enfocándose principalmente en el área tumoral, luego realizará el mismo trabajo con las láminas trazadas por inmunohistoquímica (IHC) mostrando un mapa de calor con las diferentes marcaciones obtenidas por (IHC), permitiendo al observador una excelente clasificación del tumor para su posterior tratamiento o si resulta beneficiado del tratamiento el paciente que ha sido escaneado mediante el sistema de inteligencia artificial ASI.
Bibliografía
- Keytruda [información de prescripción]. Kenilworth, NJ: Merck & Co.
- Reck M, Rodríguez-Abreu D, Robinson AG, et al. Pembrolizumab versus quimioterapia para el cáncer de pulmón de células no pequeñas PD-L1 positivo.N Engl J Med.2016;375:1823-33.
- Herbst RS, Baas P, Kim DW, et al. Pembrolizumab versus docetaxel para el cáncer de pulmón de células no pequeñas avanzado, previamente tratado, positivo para PD-L1 (KEYNOTE-010): un ensayo controlado aleatorizado.Lanceta. 2016;387(10027):1540-1550.
- Roach C, Zhang N, Corigliano E, et al. Desarrollo de un ensayo inmunohistoquímico de PD-L1 de diagnóstico complementario para la terapia con pembrolizumab en el cáncer de pulmón de células no pequeñas. Inmunohistoquímica aplicada Mol Morfología. 2016;24:392-397.
- PD-L1 IHC 28-8 Instrucciones de uso de PharmDx.
- www.agilent.com/en/product/pharmdx/pd-l1-ihc-28-8-pharmdx