El pasado 30 de mayo el Instituto Nacional de Salud (INS) publicó el documento ACTUALIZACIÓN DE LAS RECOMENDACIONES TÉCNICAS Y OPERATIVAS PARA LABORATORIOS DE TAMIZAJE NEONATAL – versión 01 el cual amplia y precisa criterios técnicos y operativos bajo los cuales deben operar los laboratorios que hacen parte del Programa de Tamizaje Neonatal en el territorio nacional, estos lineamientos aplican a:
- INS.
- Secretarias de Salud o las entidades que hagan sus veces.
- IPS.
- EPS.
- Entidades adaptadas, regímenes de excepción y especial.
- Demás entidades que desarrollan procedimientos de gestión de la atención o de atención directa al recién nacido en el marco de la atención en salud y de la operación de las Rutas Integrales de Atención en Salud.
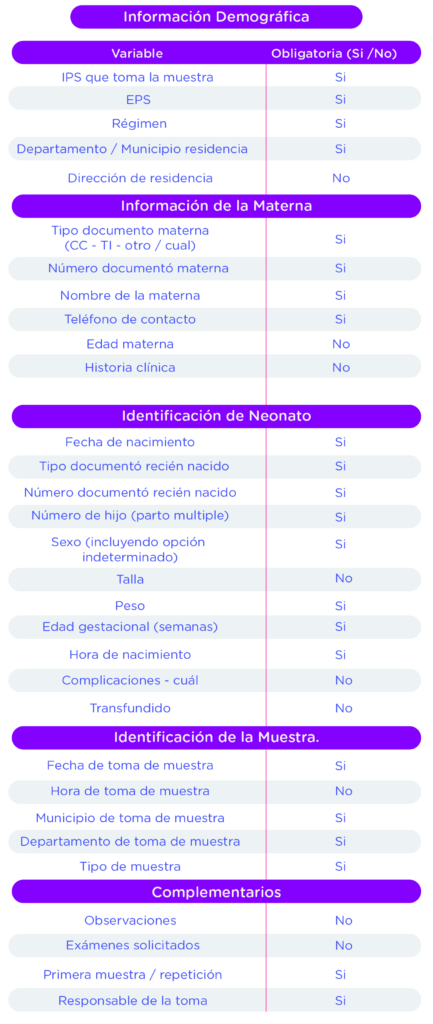
En el componente preanalítico se hace énfasis en la capacitación y seguimiento a la calidad de la muestra, así mismo, se presentan consideraciones de contenido de datos diligenciables en las tarjetas, para que los proveedores de tarjetas generen el ajuste necesario para lo cual hay plazo hasta febrero del 2026; el lineamiento indica que, mientras ello ocurre, las IPS que tomen muestras en conjunto con las IPS que las procesan, deberán definir estrategias para registrar la información a completitud, aun cuando la tarjeta comercial utilizada no cuente con ella, en el anexo se encuentra la información necesaria para la tarjeta de toma de muestra, como novedad, se hace obligatorio el registro de los documentos que identifican al menor: número el certificado de nacido vivo o NUIP.
Así mismo, se recalca la importancia de la toma de muestra de sangre de talón para avanzar hacia el tamizaje de hipotiroidismo congénito (y luego de otras patologías), para lo cual el lineamiento indica que cada IPS del país que atiende recién nacidos debe trazar un plan para garantizar la toma de muestra de sangre del talón, con el objeto de que, “en un periodo no mayor a dos años posteriores a la expedición de la Resolución 207 de 2024, se haya realizado el cambio del origen de la muestra a sangre proveniente del talón del neonato”, sin dejar de lado la oportunidad de la toma de muestra que debería hacerse entre las 24 y 72 horas posteriores al nacimiento. Frente al transporte de la muestra, se hace aclaración que la temperatura no debe superar los 20°C durante el transporte, pero la temperatura de conservación no debe superar los 8°C y debe realizarse cumpliendo los lineamientos de la IATA (International Air Transport Association) y su almacenamiento se debe garantizar por tres meses a la misma temperatura, no se aconseja la congelación a -20°C debido a que “se puede perder la capacidad de extracción por mayor retención en el papel, así que el resultado puede no ser confiable”.

Para el componente analítico, el lineamiento hace énfasis en la importancia de procesar las muestras así cuenten con baja calidad de manera que se evite el riesgo de dejar pasar un caso positivo, no obstante, si es imposible realizar el análisis, se debe informar a la IPS correspondiente. También se indica que todo laboratorio debe participar en los programas de evaluación del desempeño coordinados por el INS.
Por último, con relación al componente postanalítico, se hace énfasis en los datos requeridos en el reporte de resultados:
- Fecha de nacimiento
- Fecha de toma de muestra
- Fechas de análisis y
- Fecha de reporte de resultado de la prueba
Se debe incluir lo requerido en la ISO 15189 (Laboratorios clínicos, requisitos para la calidad y competencia) numeral 7.4.1.6. Se deben seguir los puntos de corte recomendados en la tabla 7.

ANEXO. Información requerida en la tarjeta de toma de muestra para tamizaje neonatal.